研究背景
如何實現活體組織深層光學信息的無創、快速獲取,一直備受臨床研究領域的關註。得益於靈敏度高、特異性強、指紋譜、譜峰窄等特點,表面增強拉曼光譜(SERS)技術得到了研究者們的青睞,多種SERS探針被開發並用於生物檢測和成像。然而🚖,和大多光學技術一樣🪹,由於生物組織中強烈的光子散射、吸收以及自發熒光幹擾,傳統SERS技術在獲取組織深層信息方面遇到了巨大挑戰🟪。
表面增強透射拉曼光譜(SETRS)結合了SERS和透射拉曼光譜(TRS)的優勢,通過將激光入射端和信號收集端分置於樣品的兩側,有效地抑製了表面熒光或拉曼背景信號的影響🥷🏽,提高了來自組織深處的拉曼信號的信噪比🔟。此前,葉堅教授和林俐助理教授團隊已實現厚達14cm的冷凍豬肉組織中SERS探針信號的檢測💌。此外課題組在之前的研究中曾開發了基於拉曼光譜的病竈深度預測方法,依賴於分析拉曼譜峰對強度比值(RPR)的自然對數值與病變位點深度(d)之間的線性關系⬆️,即🌊。
然而👨🏻🦲👨🏽🔬,由於生理環境的復雜性和組織類型的多樣性,SETRS在活體動物模型檢測中已知的最大深度不足1.3厘米👨🎨,其深層病竈檢測潛力仍有待開發,在活體組織中最高能測到多深,仍是未知數🏑。此外,該深度預測放法中的關鍵光學系數——光學有效衰減系數之差(Δμ)通常在冷凍樣本中測得。冷凍樣本易獲取、保存、操作👥,是組織光學研究的常用樣本。但是冷凍組織和新鮮組織之間的光學性質存在差異👩❤️💋👩,可能影響預測結果🍭。冷凍後檢測所得和新鮮組織中測得的Δμ究竟有多大差異⏪,冷凍後檢測所得Δμ是否能滿足活體復雜組織模型上的深度預測結果的準確性和穩定性,仍是未知數↪️。因此,研究冷凍對組織樣本光學性質的影響是很有必要的◾️。
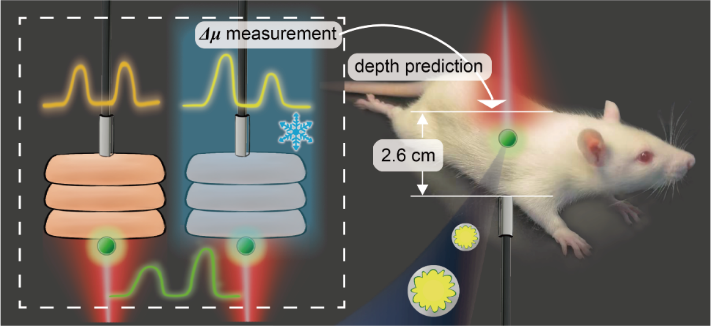
圖1 SETRS系統中🧿,使用新鮮或冷凍組織的“有效衰減系數差之差”(Δμ)預測活體大鼠病竈仿體的深度
本工作在組織結構與類型相對復雜的大鼠腹部進行了基於SETRS技術的病竈仿體深度預測,並研究了冷凍或非冷凍組織測得的光學參數對深度預測的準確性的影響(圖1)🦻🏿。為了增加在體異質模型中的穿透深度,本工作優化了縫隙增強拉曼標簽(GERTs),隨後測量了大鼠不同組織在冷凍不同時間後的Δμ值,最終比較這些Δμ對深度預測準確性的影響。具體研究思路和研究結果如下文。
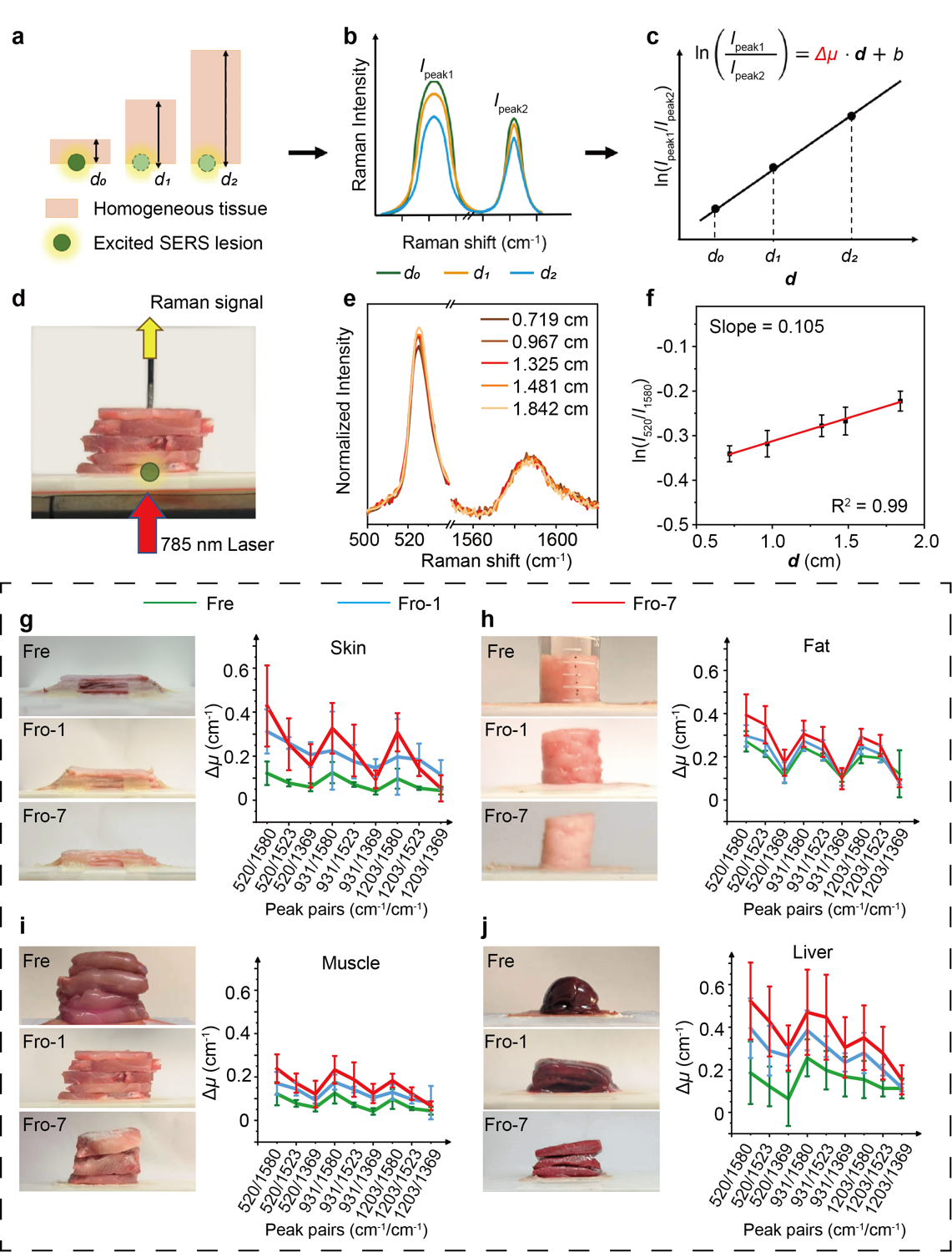
圖2 基於SETRS技術的離體樣本Δμ測量及冷凍前後Δμ的變化
該工作首先測定了大鼠四種組織(包括皮膚、肌肉、脂肪和肝臟)在新鮮、冷凍一天、冷凍七天狀態下的Δμ值🕙。圖2中👏🏼,團隊研究用肌肉組織作為示例🦩,展示了測量一種組織一個峰對的Δμ的過程🧑🏿🦰🎅🏿。首先使用TRS系統收集拉曼光譜,785 nm寬場激光束自下而上地照射在組織塊底部的SERS凝膠上,激發的拉曼光子在組織塊中傳播,最終被組織上表面接觸的光纖式拉曼探頭收集。對於同一勻質組織,團隊研究人員收集了來自五個不同深度的SERS凝膠的拉曼光譜。以520和1580 cm-1的拉曼峰對為例,其自然對數值與深度呈良好的的線性關系。最終,對於每一種組織的每種冷凍狀態,團隊研究人員分別計算了九對拉曼峰對(520/1369、520/1523🥀、520/1580🙋🏼♂️、931/1369、931/1523、931/1580、1203/1369、1203/1523💋、1203/1580)的Δμ,以研究冷凍是如何影響組織Δμ,並最終影響到組織深度預測🏊🏼♂️。
結果顯示離體組織Δμ的變化大致遵循三個趨勢𓀋:(1)在一定範圍內,Δμ隨著峰對之間波長差的大小而增加2️⃣;(2)整體而言,大部分拉曼峰對的Δμ隨著樣本冷凍時間的延長而上升;(3)在所分析的四種組織中,肝臟組織在冷凍反應中表現出最顯著的Δμ變化,而肌肉受到的的影響最小。
對於以上現象,團隊研究人員作出如下解釋🧑⚖️:(1)波長增加,生物成分表現出更強的光吸收。因此,兩個峰之間更大的拉曼位移,組織光吸收的差異更大,從而表現出更大的Δμ🕠。(2)冷凍會破壞細胞微觀結構,致使血紅蛋白轉變為含氧狀態🥵,吸收更多長波長的光🤱,導致冷凍後Δμ整體呈上升趨勢🙇🏼。(3)肝臟含有大量血液,其Δμ更容易受到冷凍的影響。
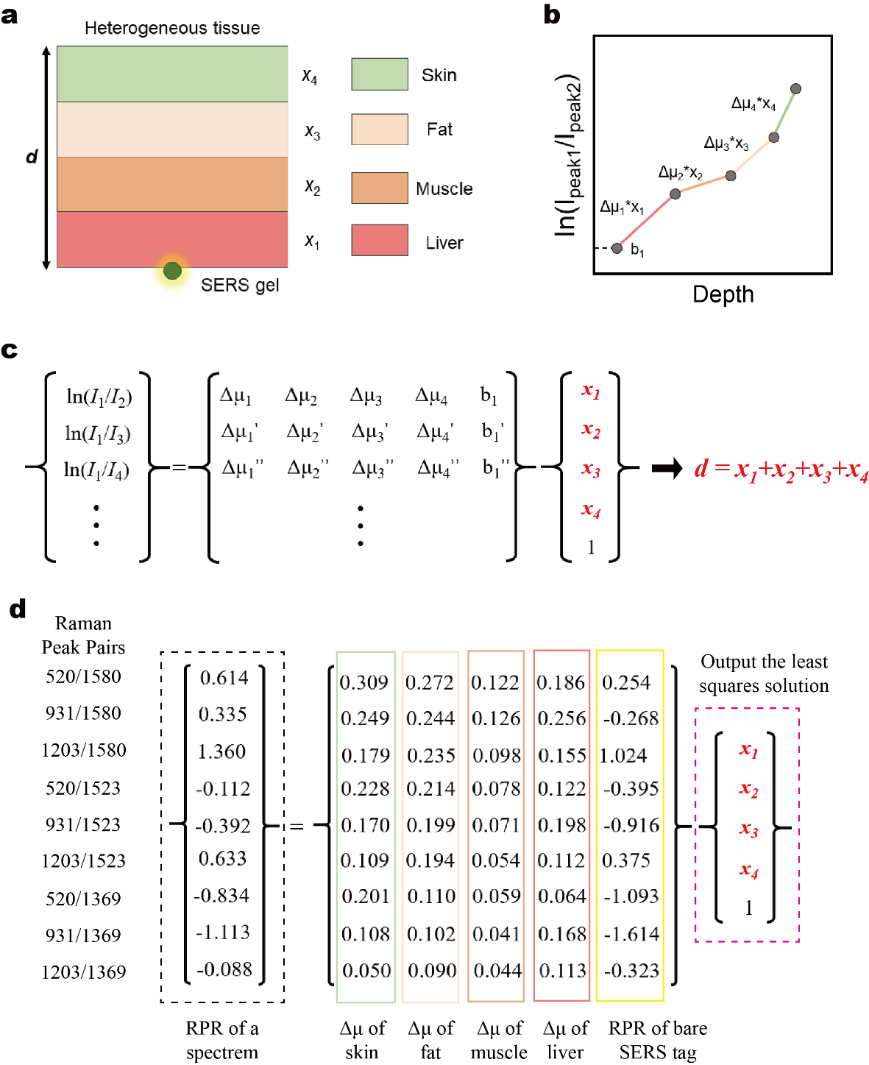
圖3 活體大鼠肝臟病竈仿體深度預測模型示意圖
接下來,團隊研究人員參考了課題組已發表的深度預測理論模型(Small Method, 2023, 7, e2201334)。在進行大鼠肝腹部深度預測時👀,拉曼光子會穿過四種不同組織(肌肉、脂肪🧑🏽💻、皮膚和肝臟),不同波長的拉曼光子構成的每個拉曼峰對有一個Δμ組(有來自同一條件測得的四種組織對應的四個Δμ值構成)。這四種組織的Δμ、拉曼光子在各個組織中走過的距離以及拉曼光子強度比值的對數值存在如圖3的關系🧎🏻♂️➡️。因此🤽🏿♂️,為了求解拉曼光子穿透的總組織深度d(即SERS凝膠深度)💸,需要構成如圖所示的超定方程,通過最小二乘法求解出x1, x2, x3, 和x4,並最終計算出預測深度d。

圖4 SETRS系統中對活體大鼠體內SERS病竈仿體進行無創檢測,並使用新鮮或冷凍組織的“有效衰減系數差之差”(Δμ)預測模擬病竈的深度
最後,利用上述深度預測模型,團隊研究人員將測得的Δμ值用於活體大鼠模型中SERS病竈仿體的深度預測👏。如圖4👵🏽,首先通過手術將SERS病竈仿體植入活體大鼠的腹部。然後,通過兩步法掃描對病竈仿體進行精準定位,並收集病竈仿體投影點及其周圍八個點的光譜信息。掃描過程中,使用光斑的激光功率密度約0.22 W/cm2,低於臨床MPE閾值(0.3 W/cm2),保證了測試過程的光安全性⌛️🧚🏼♀️。測試結束後,對大鼠進行安樂死,並通過解剖確定病竈仿體的深度🏖。
在構建深度預測超定方程時🌧👳♂️,每個Δμ組分別從新鮮樣本、一天冷凍樣本和七天冷凍樣本中獲得。綠色圖表示使用新鮮組織測量的Δμ進行預測,預測值為8.1 ± 2.7 mm,與實際深度非常接近⛹🏿♂️,偏差小於5%。相比之下,使用冷凍一天或七天組織的Δμ的預測深度分別為17.2 ± 5.8和1.7 ± 15.3 mm(淺藍色和深藍色圖)🦸🏽。這些預測與實際深度大相徑庭,深度預測相對標準偏差(RSD)超過50%。實驗證明📕,冷凍組織的Δμ值對深度預測結果影響較大,不適合用於預測復雜活體動物的深度。因此,冷凍會改變組織的光學特性,進而大幅度影響Δμ在組織深度預測中的適用性。
總體而言,本工作采用高亮度的縫隙增強拉曼探針,最終實現了在活體復雜生物模型中整體光學穿透深度達2.6 cm,目標病竈仿體深度超過0.8 cm的準確深度預測🐬🧔。研究還發現經過冷凍的樣本,其Δμ值會明顯改變,進而影響到深度預測的準確性🧎🏻♀️🧖🏿♂️。這項工作推動了 SERS 領域的發展,有助於在高度復雜的活體模型中進行深度預測研究🚣🏻♀️🤹🏿♀️,並填補了拉曼領域在光學系數研究方面的空白。此外,本工作還研究了冷凍對樣品和光學深度預測技術的影響,從而拓展了 SETER 系統在體內生物醫學應用方面的潛力。總的來說,用於深度預測的 SETER 在臨床應用方面很有前景。
意昂4体育平台碩士生周羽彤為本文的第一作者。意昂4体育平台林俐助理教授和葉堅教授為本文的共同通訊作者。該研究工作得到了國家自然科學基金委、上海婦科腫瘤重點實驗室、意昂4平台醫工交叉合作基金的支持。這項工作也獲得了由上海市教育委員會 “晨光計劃”的支持。
葉堅教授課題組主頁:http://www.yelab.sjtu.edu.cn